الهدف 3: ضمان حياة صحية جيدة
https://sdgs.un.org/goals/goal3
أ.م.د. نور عبد الامير عوده
قسم الفيزياء الطبية ،كلية العلوم الطبية التطبيقية ،جامعة كربلاء ،كربلاء ،العراق .
البريد الإلكتروني: noor.a.oda@uokerbala.edu.iq
* تدعم العلاجات الخلوية المبتكرة المتمثلة بالخلايا التائية المهندسة جينياً هدف التنمية المستدامة الثالث عبر خفض الوفيات وتوفير حلول علاجية عادلة ومنخفضة التكلفة. كما تساهم هذه العلاجات الجذرية في تخفيف الأعباء الاقتصادية على الأنظمة الصحية، مما يعزز استدامة الموارد وتوسيع التغطية الشاملة.
الملخص
تُعدّ الخلايا المناعية التائية المنظِّمة (T-regs) عنصرًا محوريًا في الحفاظ على الاتزان المناعي والتحمّل الذاتي. وقد أتاحت التطورات الحديثة في هندسة الجينوم لا سيما باستخدام تقنية CRISPR-Cas 9 إنتاج خلايا T-regs معدَّلة وراثيًا تتمتع بثبات ووظيفة وانتقائية أعلى. إن توظيف هذه الخلايا كـ«علاجات ذكية» يمثّل تحولًا نوعيًا من العلاج بطريقة التثبيط المناعي الشامل إلى التنظيم المناعي الموضعي والموجّه نوعيًا. يستعرض هذا المقال الأساس البيولوجي لوظيفة T-regs، ومبررات استخدامها كمنصات توصيل خلوية، واستراتيجيات هندستها،وتطبيقاتها العلاجية في أمراض المناعة الذاتية وزراعة الأعضاء، إضافةً إلى التحديات التقنية والتنظيمية المرتبطة بها.
المقدمة:
يُعد الجهاز المناعي البشري منظومة بيولوجية بالغة التعقيد، تتمثل وظيفتها الفسيولوجية الأساسية في التمييز الدقيق بين مستضدات “الذات” (خلايا الجسم السليمة) و”اللاذات” (العوامل الممرضة الخارجية). ومع ذلك، قد يحدث خلل وظيفي في آليات التحمل المناعي ، مما يؤدي إلى استجابة مناعية مفرطة وغير طبيعية، تهاجم فيها الخلايا المناعية أنسجة الجسم السليمة وتؤدي إلى تلفها[1] . يُعرف هذا الخلل سريرياً بأمراض المناعة الذاتية ، والتي تشمل مجموعة واسعة من الحالات الطبية مثل داء السكري من النوع الأول والتصلب اللويحي. وفي الوقت الحاضر، يشهد الحقل الطبي تحولاً جذرياً في مقاربة هذه الأمراض [2] ؛ إذ تتجه الأبحاث بعيداً عن الاستراتيجيات التقليدية القائمة على التثبيط العام وغير الموجه للجهاز المناعي، نحو نهج أكثر تخصصاً يهدف إلى “إعادة برمجة” الاستجابة المناعية وتعديلها على المستوى الخلوي والجزيئي، وذلك بالاعتماد على أدوات التحرير الجيني المتقدمة، وعلى رأسها تقنية CRISPR-Cas9 وكما هو موضح في الشكل (1).
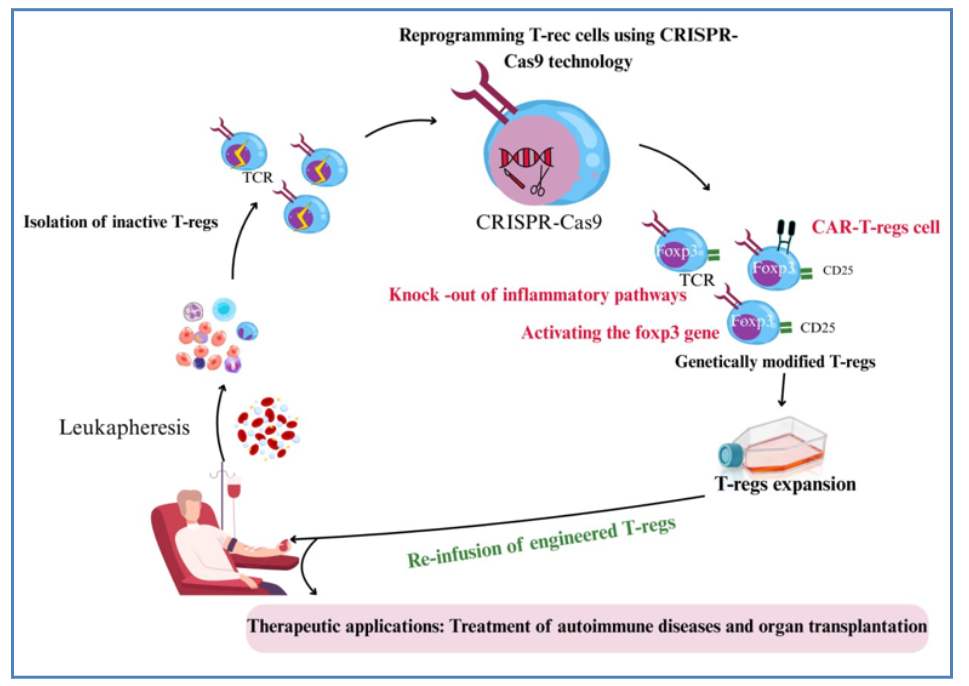
الشكل (1): مسار التصنيع الحيوي للعلاج المناعي الخلوي المتمثل بمنصات الخلايا التائية التنظيمية المُهندسة وراثياً باستخدام تقنية CRISPR-Cas 9.
1- الأساس البيولوجي لعمل خلايا (Tregs) وآليات التحمل المناعي
- الدور الفسيولوجي: تُشكل الخلايا التائية التنظيمية نسبة تتراوح بين 5-10% من إجمالي الخلايا التائية المحيطية. وتُعد الركيزة الأساسية للحفاظ على الاستتباب المناعي Immune Homeostasis) ( والتحمل المحيطي، حيث تمنع الاستجابات الالتهابية المفرطة وتلف الأنسجة عبر إفراز سيتوكينات مثبطة قوية، أبرزها (IL-10) و [3].(TGF-β)
- بروتينFOXP3 كالمنظم الرئيسي: يُحدد عامل النسخ النووي (FOXP3) الهوية الخلوية والوظيفة الكابحة للخلايا التائية التنظيمية. يعمل هذا البروتين بآلية مزدوجة؛ حيث يُحفز التعبير عن الجينات الكابحة الحيوية مثل CD25 و CTLA-4 بينما يُثبط بشكل صارم التعبير عن السيتوكينات الالتهابية مثل IL-2 و. IFN-γ [4]
- الإمراضية في المناعة الذاتية: تنشأ أمراض المناعة الذاتية عند انهيار هذا النظام التنظيمي. يؤدي النقص الكمي أو الخلل الوظيفي في خلايا T-regs والذي ينتج غالباً عن طفرات في جين FOXP3 أو التعرض لبيئات نسيجية شديدة الالتهاب إلى فقدان السيطرة المناعية، مما يسفر عن استجابات هجومية غير مقيدة من الخلايا التائية ضد المستضدات الذاتية وتدمير تدريجي للأنسجة. [5]
2- الآليات والمبررات العلمية لاستخدام الخلايا التائية التنظيمية كمنصات خلوية واعدة في علاج الامراض المناعية
يُمثل توظيف الخلايا التائية التنظيمية المُهندسة وراثياً كـ “منصات حية” قابلة للبرمجة تحولاً جذرياً في مسار علاج الأمراض المناعية، حيث تقدم مزايا دوائية حاسمة تتفوق على علاجات التثبيط المناعي الجهازية التقليدية ومن هذه المزايا:
- الانجذاب النسيجي والتوجيه الدقيق :(Targeted Tissue Homing) تتميز هذه الخلايا بقدرتها الفائقة على التوجه بدقة نحو مواقع المرض؛ حيث يتم تزويدها بمستقبلات مُهندسة مثل CARs أو TCRs تعمل كـ أنظمة استهداف جزيئي متطورة تتيح لها تتبع الإشارات الكيميائية في الجسم والهجرة مباشرة نحو الأعضاء الملتهبة، مثل البنكرياس في حالة السكري من النوع الأول أو المفاصل في حالة التهاب المفاصل الروماتويدي. ويضمن هذا التمركز الموضعي الدقيق معالجة الخلل المناعي في مكانه دون التأثير على باقي أجزاء الجسم، مما يقي المريض من الآثار الجانبية الخطيرة المرافقة لأدوية التثبيط المناعي العام[6].
- التثبيط الموضعي الجانبي :(Localized Bystander Suppression) بمجرد التعرف على المستضد، تُفرز خلايا Tregs سيتوكينات مثبطة قوية مثل IL-10 و TGF-β و IL-35 والأهم من ذلك، أنها تمتلك خاصية “التثبيط الجانبي”؛ حيث تكبح بفعالية كافة الخلايا التائية المستجيبة المجاورة داخل البيئة الدقيقة للالتهاب، بغض النظر عن نوع المستضدات التي تستهدفها تلك الخلايا. [7]
- الاستدامة الخلوية: (Cellular Sustainability) على النقيض من الأدوية التقليدية التي تتطلب جرعات مستمرة لتعويض التصفية الاستقلابية (Metabolic Clearance) التي تحدث لجرعة الدواء في الجسم ، تُعد خلايا T-regs “منصات علاجية حية” قادرة على التكاثر الذاتي. فهي تستمر داخل الجسم الحي لفترات طويلة، مما يوفر فعالية علاجية مستدامة ويفتح المجال لاستعادة التحمل المناعي بشكل دائم [8] .
- حمولات علاجية قابلة للتخصيص : (Customizable Therapeutic Payloads) تتيح أدوات التحرير الجيني المتقدمة مثل CRISPR-Cas9 تسليح خلايا T-regs بقدرات حيوية إضافية. إذ يمكن هندستها لإيصال إنزيمات مرممة للأنسجة المتضررة، أو تزويدها بـ “مفاتيح أمان تضمن القضاء السريع عليها في حال ظهور أي مضاعفات سريرية غير مرغوبة. [9]
3- استراتيجيات تعديل الجينوم في خلايا T-regs
لقد أتاحت تقنية CRISPR-Cas9 إمكانات غير مسبوقة لإعادة برمجة خلايا T-regs، وتتركز هذه الاستراتيجيات في أربعة محاور رئيسية:
1- إدخال جينات علاجية بشكل موجَّه :(Targeted Gene Insertion) لا يقتصر دور CRISPR على “قص” الجينات المعيبة، بل يُستخدم لإدخال جينات جديدة تمنح الخلايا قدرات إضافية. أشهر تطبيق لذلك هو إدخال جينات “مستقبلات المستضد الخيمرية” (CAR) لتوجيه خلايا T-regs نحو نسيج معين (مثل البنكرياس أو الكبد) بدقة متناهية، بدلاً من الدوران العشوائي في الدم [10] .
2- تعطيل مسارات التهابية محددة :(Knock-out of Inflammatory Pathways) في البيئات شديدة الالتهاب (كما في أمراض الروماتيزم)، قد تفقد خلايا Tregs هويتها وتتحول إلى خلايا التهابية هجومية. لتجنب ذلك، يتم استخدام المقص الجيني لتعطيل المستقبلات التي تستجيب للسيتوكينات الالتهابية، مما يضمن بقاء الخلايا وفية لوظيفتها الكابحة . [11]
3- تعزيز استقرار الجين :FOXP3 يُعد جين FOXP3 “المايسترو” الذي يُعرّف الخلية التنظيمية ويحافظ على وظيفتها. يتم استخدام التعديل الجيني لمنع إسكات هذا الجين (Epigenetic silencing)، مما يضمن بقاء الخلايا مستقرة وقوية حتى في أشرس البيئات المرضية [12].
4- إدخال حمولة علاجية في “مواقع جينومية آمنة” (Safe Harbors): عند إدخال جين جديد، هناك خطر من أن يندمج في مكان يعطل جيناً مهماً آخر (مما قد يسبب السرطان). لذا، تُوجه تقنية CRISPR لإدخال الجينات العلاجية في مواقع تُعرف بـ “الملاذات الآمنة في الجينوم” (مثل موقع AAVS1)، حيث يمكن للجين الجديد التعبير عن نفسه بأمان دون الإضرار بوظائف الخلية الأساسية. [13]
4- التطبيقات السريرية لمنصات (T-regs) الخلوية الذكية
تتركز التطبيقات العلاجية للخلايا التائية التنظيمية المُهندسة وراثياً في إحداث تثبيط مناعي موضعي وموجه، وتُصنف سريرياً عبر المحاور التالية:
- زراعة الأعضاء: (Organ Transplantation) من خلال توجيه خلايا CAR-Tregs للتعرف على مستضدات المتبرع HLA لتأسيس تحمل مناعي موضعي يمنع رفض الطعم ويُقلل الاعتماد على مثبطات المناعة الجهازية.
- السكري من النوع الأول :(T1D) توجيه الخلايا نحو البنكرياس لحماية خلايا “بيتا” من التدمير المناعي ، للحفاظ على الكتلة المفرزة للأنسولين.
- التصلب المتعدد :(MS) استهداف مستضدات الميالين في الجهاز العصبي المركزي لكبح الالتهاب العصبي وتوفير بيئة داعمة لإعادة الميالين. (Remyelination)
- الأمراض الالتهابية المزمنة مثل داء التهاب المفاصل الروماتويدي و الأمعاء الالتهابي: حصر التأثير الكابح في الغشاء الزليلي أو المخاطي، مع توظيف تقنية (CRISPR) لمنع التحول المظهري (Phenotypic Conversion) لهذه الخلايا عند تعرضها لبيئات نسيجية شديدة الالتهاب.
التحديات العلمية وعقبات التصنيع الحيوي
على الرغم من الآفاق السريرية الواعدة لعلاجات خلايا T-regs المُهندسة، إلا أنها تواجه تحديات علمية وعقبات في التصنيع الحيوي تعيق تطبيقها على نطاق واسع. تتمثل أولى هذه التحديات في “المرونة المظهرية”، حيث قد تفقد هذه الخلايا وظيفتها الكابحة للمناعة في البيئات شديدة الالتهاب وتتحول إلى خلايا ممرضة مثل خلايا Th-17 ، مما يُحتم إجراء تعديلات متقدمة كالتثبيت الفوق-جيني لجين FOXP3لضمان استقرارها. إلى جانب ذلك، تبرز عقبات التصنيع المتمثلة في الاعتماد الحالي على الخلايا الذاتية للمريض نفسه، وهو مسار باهظ التكلفة، ويستغرق وقتاً طويلاً، ويصطدم سريرياً بضعف جودة الخلايا المستخلصة من مرضى يعانون أساساً من خلل مناعي. وأخيراً، يفرض استخدام تقنية (CRISPR-Cas9) مخاطر تتعلق بالسلامة بسبب احتمالية حدوث طفرات جينومية في مواقع غير مستهدفة، مما قد يؤدي إلى تعطيل الجينات الكابحة للأورام أو تنشيط الجينات المسرطنة.
الخلاصة
تُحدث هندسة الخلايا المناعية T-regs باستخدام تقنية التعديل الجيني CRISPR-Cas9 ثورة طبية في علاج أمراض المناعة الذاتية وزراعة الأعضاء. ويمكن تلخيص هذا التحول في النقاط التالية:
- علاج موجه بدلاً من إضعاف المناعة: بدلاً من استخدام أدوية تثبط جهاز المناعة بأكمله وتجعل المريض عرضة للعدوى، تهدف هذه التقنية إلى “تدريب” جهاز المناعة ليكون متسامحاً ويتوقف عن مهاجمة الجسم أو الأعضاء المزروعة.
- تجاوز عقبات الإنتاج: على الرغم من وجود تحديات حالية، مثل صعوبة إنتاج هذه الخلايا بكميات ضخمة أو الحفاظ على استقرارها، إلا أن الأبحاث تتسارع لتطوير “علاجات خلوية جاهزة للاستخدام” يمكن إنتاجها بسهولة لتجاوز هذه العقبات.
- شفاء مستدام ودعم للاقتصاد: إن نجاح هذه “العلاجات الحية” وتطبيقها الفعلي في المستشفيات لن يمنح المرضى شفاءً حقيقياً وطويل الأمد فحسب، بل سيقلل أيضاً من التكاليف المالية الباهظة المرتبطة بعلاج الأمراض المزمنة، مما يصب مباشرة في صالح أهداف التنمية المستدامة .
دليل المصطلحات والمختصرات الواردة في المقال
- = T-regs الخلايا المناعية التائية المنظِّمة وظيفتها الحفاظ على الاتزان والتحمل المناعي.
- = CRISPR-Cas9 تقنية التحرير الجيني أو “المقص الجيني” تُستخدم لإعادة برمجة وتعديل جينوم الخلايا.
- = FOXP3عامل النسخ النووي هو البروتين المنظم الرئيسي الذي يُحدد الهوية والوظيفة الكابحة لخلايا T-regs.
- = IL-10 إنترلوكين 10 (سيتوكين بروتيني مثبط تفرزه الخلايا لكبح الالتهاب).
- = TGF-β عامل النمو المحول بيتا (سيتوكين مثبط لمنع تلف الأنسجة).
- = IL-35 إنترلوكين 35 (سيتوكين مثبط يساعد في التثبيط الموضعي للخلايا المجاورة).
- = CD25 / CTLA-4 جينات ومستقبلات كابحة حيوية (يعزز بروتين FOXP3 ظهورها لأداء الوظيفة التنظيمية).
- = IL-2 / IFN-γ سيتوكينات التهابية (بروتينات محفزة للالتهاب يتم تثبيطها بواسطة خلايا T-regs ).
- = CARs مستقبلات المستضد الخيمرية (مستقبلات مُهندسة تُضاف للخلايا لتوجيهها بدقة نحو نسيج معين).
- = TCRs مستقبلات الخلايا التائية (مستقبلات تُستخدم لتعزيز التوجيه الدقيق للخلايا نحو مواقع المرض).
- = AAVS1 موقع جينومي آمن (مكان آمن في الحمض النووي لإدخال الجينات العلاجية دون التسبب بأضرار أو أورام).
- = HLA مستضدات الكريات البيضاء البشرية (مستضدات المتبرع التي يتم توجيه الخلايا للتعرف عليها لمنع رفض زراعة الأعضاء).
- = T1D السكري من النوع الأول (مرض مناعي ذاتي يهاجم خلايا البنكرياس) .
- = MS التصلب المتعدد أو اللويحي (مرض مناعي يهاجم مستضدات الميالين في الجهاز العصبي).
- = Th-17 خلايا تائية مستجيبة ممرضة (خلايا التهابية هجومية قد تتحول إليها خلايا T-regs إذا فقدت استقرارها).
المراجع:
1. Han L, Wu T, Zhang Q, Qi A, Zhou X. Immune tolerance regulation is critical to immune homeostasis. J Immunol Res. 2025;2025(1):5006201. Available from: http://dx.doi.org/10.1155/jimr/5006201
2. Popoviciu MS, Kaka N, Sethi Y, Patel N, Chopra H, Cavalu S. Type 1 Diabetes Mellitus and autoimmune diseases: A critical review of the association and the application of personalized medicine. J Pers Med. 2023;13(3):422. Available from: http://dx.doi.org/10.3390/jpm13030422
3. Dikiy S, Rudensky AY. Principles of regulatory T cell function. Immunity [Internet]. 2023;56(2):240–55. Available from: http://dx.doi.org/10.1016/j.immuni.2023.01.004
4. Inandiklioglu N. AN OVERVIEW OF THE FOXP3 GENE AND REGULATORY T CELLS. Current Studies in Medical Biology and Genetics. 2025;II.
5. Xie W-W, Huang J-B, Zhou Y-C, Yuan J-Y, Feng J-X, Shi X-H, et al. The immunobiology and therapeutic potential of regulatory T cells in autoimmune diseases and allergic diseases. Front Immunol. 2025;16(1709915):1709915. Available from: http://dx.doi.org/10.3389/fimmu.2025.1709915
6.Yang Y, Liu J, Liu J, Wei S, Kong X, Mu W, et al. Advances in immune cell-based therapeutic agents for the treatment of inflammation-related diseases. Acta Pharm Sin B. 2026; Available from: http://dx.doi.org/10.1016/j.apsb.2026.01.013






























































